A two-years real-word study with fingolimod: early predictors of efficacy and an association between EBNA-1 IgG titers and multiple sclerosis progression
Maria Inmaculada Dominguez-Mozo, Victoria Galán, Lluís Ramió-Torrentà, Ana Quiroga, E Quintana, Luisa María Villar, Lucienne Costa-Frossard, José Ignacio Fernández-Velasco, Noelia Villarrubia, María Angel Garcia-Martinez, Rafael Arroyo, Roberto Alvarez-Lafuente.
La identificación de factores predictivos y biomarcadores tempranos es de gran importancia para evitar futuros fracasos terapéuticos. Fingolimod ha demostrado ser un tratamiento eficaz en la reducción de la tasa de brotes y también en la ralentización de la progresión de la discapacidad en pacientes con esclerosis múltiple (EM) remitente-recurrente. El objetivo principal del estudio, realizado en colaboración entre investigadores del IdISSC, el Hospital Universitario de Toledo, el Instituto de Investigación Biomédica de Girona, el Hospital Universitario QuirónSalud y el Hospital Universitario Ramón y Cajal, fue evaluar diferentes factores clínicos, radiológicos, genéticos y ambientales como posibles predictores tempranos de respuesta en pacientes con EM tratados con fingolimod durante 24 meses. Además, analizamos la posible contribución de los factores ambientales analizados a la progresión y actividad de la enfermedad a lo largo de los 2 años de seguimiento.
Con este fin, se realizó un estudio con 151 pacientes diagnosticados de EM, en tratamiento con fingolimod durante 24 meses, para los que teníamos muestras de suero al inicio del tratamiento y seis meses después, y datos clínicos y radiológicos al inicio del tratamiento y 24 meses después. Se recogieron distintas variables clínicas y radiológicas con las que se trató de identificar, por un lado, a aquellos pacientes libres de brotes, de progresión de la discapacidad y sin nuevas lesiones en resonancia magnética (RM) a lo largo de los dos años de tratamiento, es decir, aquellos pacientes sin evidencia de actividad de la enfermedad (NEDA-3, de sus siglas en inglés), y por otro lado, a aquellos que presentaban evidencia de actividad de la enfermedad a pesar del tratamiento que estaban recibiendo (EDA, de sus siglas en inglés). Además, también se analizaron los niveles de anticuerpos IgG frente a EBNA-1 y VCA del virus de Epstein-Barr (EBV) y los títulos de anticuerpos IgG e IgM contra el herpesvirus humano 6A/B (HHV-6A/B).
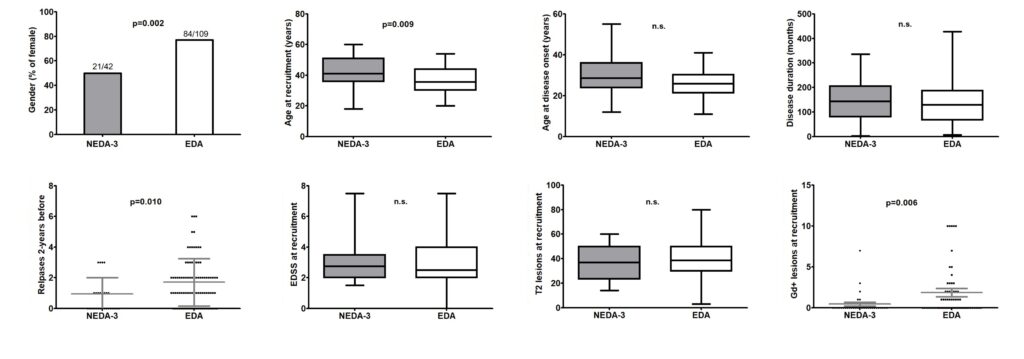
De los 151 pacientes con EM, el 27,8% fueron NEDA-3, asociándose los siguientes predictores tempranos de manera significativamente estadística con esta condición al comienzo del tratamiento: sexo (masculino; p = 0,002), edad (p = 0,009), ausencia de brotes 2 años antes (p = 0,010) y ausencia de lesiones que realzan gadolinio en RM (p=0,006). Respecto a la posible contribución de los factores ambientales incluidos en el estudio a la actividad o progresión de la enfermedad, encontramos que los títulos de IgG frente a EBNA-1 disminuyeron tan solo en el 20,0% de los pacientes que presentaban una progresión independiente de los brotes (PIRA, de sus siglas en inglés) frente al 73.3% de los pacientes cuya progresión estaba relacionada con la presencia de brotes (RAW, de sus siglas en inglés) (p=0,006; O.R.=11,0).
Por tanto, en este estudio definimos una serie de predictores tempranos que podrían ayudar a identificar a aquellos pacientes que tienen una mayor probabilidad de ser respondedores óptimos a fingolimod. Además, describimos un distinto comportamiento del EBV en función del tipo de progresión presente en la enfermedad, lo que podría ayudar en un futuro a comprender mejor el papel que este virus podría estar desempeñando en la EM.